冯丽娟 杨怀玉* 王福会
中国科学院金属所 金属腐蚀与防护国家重点实验室, 沈阳, 110016
Email: Hyyang@imr.ac.cn
个人简介
杨怀玉,博士。1986年毕业于兰州大学化学系,1991年获硕士学位,1999年获中科院金属腐蚀与防护研究所工学博士。2004年12月- 2005年12月在美国俄亥俄州立大学Fontana腐蚀中心做访问学者。
1986-1991年,在河南化学研究所从事溶液化学理论研究,在国家自然科学基金和河南省自然科学基金支持下,先后开展了氨基酸/盐水溶液中体积性质、脂肪醇与极性溶剂二元体系过量体积和超额焓的研究。
1991,7-1999,5,在中国科学院金属腐蚀与防护研究所从事腐蚀与防护基础研究工作。
1999,6-至今,在中国科学院金属研究所,主要从事材料腐蚀与防护基础或应用基础研究工作。
先后承担和负责完成20多项科研课题,其中包括国家自然科学基金、国家重点基础研究(973)、国家科技支撑计划和国家重点科研项目各1项;中国石油天然气总公司重点科研项目1项,中国石油化工总公司科研项目3项; 中国石油天然气总公司、海洋石油总公司和中科院重点项目和国际合作研究项目多项。获中科院科学技术进步二等奖1项。在国内外期刊或国际会议发表研究论文近百篇。申请国家发明专利3项。
目前担任中国腐蚀与防护学会缓蚀剂专业委员会副主任;中国腐蚀与防护学会建筑工程专业委员会 委员。

杨怀玉
摘要:本文将3种含氧有机物(山梨醇、葡萄糖和抗坏血酸)分别与十二烷基苯磺酸钠(SDBS)进行复配,利用线性极化、动电位扫描和电化学阻抗谱技术,在 3.5% NaCl 饱和 Ca(OH)2 溶液中对复配缓蚀剂的缓蚀性能进行了研究, 结合量子化学计算分析了复合物对钢筋的缓蚀协同机理。结果表明, 碱性氯离子溶液中3种含氧化合物对钢筋的缓蚀性能按山梨醇<葡萄糖<抗坏血酸顺序递增,当它们与SDBS以不同比例复配时均表现出良好的缓蚀协同效应,这种缓蚀协同作用与化合物作为路易斯碱的硬度相关;即当软硬酸碱的配比适当时,可获得较好的缓蚀效果。其中,以抗坏血酸与SDBS间协同效应最好。
关键词:钢筋腐蚀; 阻锈剂; 协同作用; 量子化学计算
1 引言
随着我国海洋开发战略的实施,大量钢筋混凝土结构在海港、码头、桥梁等工程中得到应用。然而,在海洋环境条件下,因海水的侵入容易引起混凝土中钢筋的锈蚀,使得混凝土结构在远没达到设计使用寿命时就过早失效[1]。这不仅给相关部门造成较大的经济损失,而且给相关人员的安全带来隐患。因此,如何解决混凝土中钢筋的腐蚀防护问题,对实现钢筋混凝土结构的高性能和耐久性,具有重要的工程意义。国内外普遍认为,使用缓蚀剂是一种高效、经济和易于操作的重要手段,已经成为美国混凝土协会推荐的钢筋腐蚀防护重点技术之一[2]。然而,传统无机盐类缓蚀剂因用量大、毒性高和环境污染等问题,在许多发达国家其应用已受到严格限制。近年来,开发无毒、环保的有机缓蚀剂以用来部分或全部替代无机盐类化合物已成为一种必然趋势。H. E. Jamil等研究了醇胺类有机物对钢筋的缓蚀作用,发现当添加浓度为水泥用量的4%时,钢筋的腐蚀速率可降低近2个数量级[3];Xin Zhou等开发了一种离子液体作为碱性盐水溶液中的缓蚀剂,当用量仅为0.38 mmol/L 时,缓蚀效率就高达89%[4];F. Wombacher[5]与S Martinez[6]等也分别对有机醇和氨基酸类化合物的缓蚀性能进行了研究,结果表明碱性溶液中富含N、O杂原子的有机物可有效抑制钢筋的腐蚀。然而,通常情况下单一缓蚀剂对钢筋腐蚀的抑制效果非常有限[7],若利用各组分间的缓蚀协同效应,通过适当地复配,不仅可有效提高缓蚀剂的缓蚀效果,而且可降低使用成本。为此,本文将3种富含氧有机物(即山梨醇(S)、葡萄糖(G)、抗坏血酸(A))分别与十二烷基苯磺酸钠(SDBS)进行复配,利用线性极化、动电位极化和电化学阻抗技术,在3.5% NaCl 饱和Ca(OH)2 溶液中对复配物的缓蚀性能进行了研究,并结合量子化学计算,分析探讨了复配物对钢筋的缓蚀作用机理。以期为未来缓蚀剂在实际工程中的应用提供理论和技术基础。#p#分页标题#e#
2 实验方法
腐蚀介质为空白和添加不同浓度缓蚀剂的3.5% NaCl 饱和Ca(OH)2 溶液, 由二次蒸馏水和 NaCl、Ca(OH)2 配制而成。所有试剂均为分析纯。实验温度为室温,所用缓蚀剂总浓度为 2 mmol/L。
电化学实验在Parstat 2273系统上进行。工作电极(Ф 8 × 8 mm)由普通建筑钢筋制成,除0.5 cm2工作面外,电极其余部分用牙托树脂密封。实验前将工作电极用砂纸逐级打磨至800#,蒸馏水清洗,丙酮除油后放于干燥器内备用。实验采用三电极体系,钢筋电极为工作电极,铂片作辅助电极,饱和甘汞电极(SCE)为参比电极。电极在腐蚀介质中浸泡3天后进行电化学测量。交流阻抗测量在开路电位(OCP)下进行,测量频率范围为100 kHz至10 mHz,激励信号幅值为10 mV。实验结果用ZsimpWin软件分析。线性扫描在相对OCP ±20 mV范围内进行,扫描速度为0.166 mV/s.动电位极化从相对开路电位-250 mV始,至出现明显的点蚀止,扫描速度为1mV/s。文中所有电位均相对于SCE。
量子化学计算通过 Hyperchem 7.5软件进行, 利用半经验 PM3 方法对化合物结构进行优化, 优化能量误差小于 0.01 kJmolÅ。
3 实验结果与分析
3.1 线性极化结果
表1为钢筋电极在空白和添加不同缓蚀剂3.5% NaCl饱和Ca(OH)2 溶液中的线性极化结果。腐蚀电流密度(icorr)和缓蚀效率(IE)由式(1)和(2)计算[8],其中,考虑到钢筋在3.5% NaCl饱和Ca(OH)2 溶液中处于活性溶解状态,B值取26 mV。
表1由线性极化得到的钢筋电极在3.5% NaCl饱和Ca(OH)2 溶液中的电化学参数
| System | Ratio | Rp(kΩcm2) | I (μAcm–2) | IE(%) | System | Ratio | Rp(kΩcm2) | I (μAcm–2) | IE(%) |
| Blank | 3.9 | 6.7 | G+ SDBS | 1:3 | 46.0 | 0.6 | 91.5 | ||
| S | 14.1 | 1.8 | 72.3 | G+ SDBS | 1:1 | 31.1 | 0.8 | 87.5 | |
| SDBS | 37.6 | 0.7 | 89.6 | G+ SDBS | 3:1 | 24.5 | 1.1 | 84.1 | |
| S+ SDBS | 1:3 | 76.1 | 0.3 | 94.9 | A | 76.4 | 0.3 | 94.9 | |
| S+ SDBS | 1:1 | 38.0 | 0.7 | 89.7 | A+ SDBS | 1:3 | 65.4 | 0.4 | 94.0 |
| S+ SDBS | 3:1 | 30.0 | 0.9 | 87.0 | A+ SDBS | 1:1 | 126.0 | 0.2 | 96.9 |
| G | 42.0 | 0.6 | 90.7 | A+ SDBS | 3:1 | 46.5 | 0.6 | 91.6 |
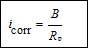 (1)
(1)
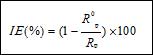 (2)
(2)
式中R0p和Rp分别为钢筋电极在空白和添加不同浓度缓蚀剂溶液中的极化电阻。
从表 1 可以看出,与空白溶液相比,添加缓蚀剂后钢筋的极化电阻大大增加,腐蚀电流密度显着减小,表明无论单一化合物,还是所复配的缓蚀剂均对钢筋的腐蚀具有一定的抑制作用。3种含氧化合物对钢筋的缓蚀效果按山梨醇<葡萄糖<抗坏血酸顺序递增。对于复配后的缓蚀剂,在实验范围内,其缓蚀效果并非随含氧化合物组份的增加而增大。具体看,当山梨醇与SDBS在摩尔比为 1:3 时,可获得最高94.9 %的缓蚀效率;而葡萄糖与SDBS在摩尔比为1:3时的最大缓蚀效率为91.5 %;抗坏血酸与SDBS的配比为1:1时可得到最高96.9 %的缓蚀效率。其中,抗坏血酸与SDBS复配时缓蚀效果最好。这表明强碱性氯离子溶液中3种含氧化合物与SDBS间存在良好的缓蚀协同效应。
3.2 动电位极化
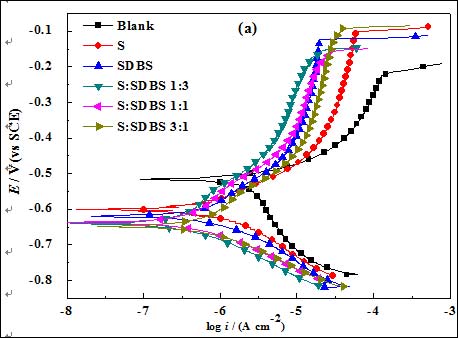
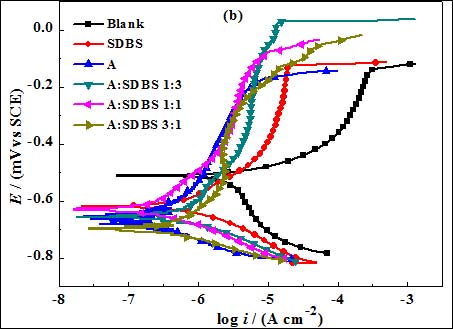
图 1. 空白和添加不同缓蚀剂时3.5% NaCl 饱和Ca(OH)2 溶液中钢筋电极的极化行为
图 1 为空白和添加不同缓蚀剂后 3.5% NaCl 饱和 Ca(OH)2 溶液中钢筋电极的极化曲线,其中,图1(a) 为山梨醇与SDBS复配后钢筋电极的极化结果,图1(b) 为抗坏血酸与SDBS复配后的实验结果;鉴于葡萄糖与SDBS复配后的极化特征与山梨醇和SDBS复配后极化行为相类似,其动电位极化结果没有给出。表2为Tafel线性拟合得到的相关电化学参数。由图1可以看出,添加缓蚀剂后, 体系的阴、阳极腐蚀过程均受到抑制,极化曲线向低腐蚀电流密度方向偏移,但缓蚀剂对钢筋阴极过程的抑制明显要强于阳极, 且添加缓蚀剂后,钢筋电极的点蚀电位均高于空白体系,表明缓蚀剂的添加提高了钢筋电极的阴阳极的极化过程和耐氯离子的侵蚀性能,缓蚀剂对钢筋的腐蚀具有明显的抑制作用。与空白体系相比,添加所有缓蚀剂后,电极的腐蚀电位明显负移 (见表2),表明所研究的缓蚀剂主要是通过对阴极氧还原过程的抑制而发挥作用,为阴极型缓蚀剂。这是因为一方面含氧化合物分子和磺酸根离子可与溶液中氯离子在钢筋表面发生竞争吸附,另一方面由于缓蚀剂分子具有良好的鳌合性能,可与钢筋电极表面腐蚀形成的 Fe2+或Fe3+离子形成不溶性络合物而覆盖在电极表面,从而阻滞阴极氧的还原和阳极铁的活性溶解[9]。#p#分页标题#e#
另外,仔细观察图1(a)可以发现,与空白溶液相比,钢筋电极的阳极极化行为具有以下特征:在阳极极化的初期,钢筋的活性溶解受到抑制,而后随阳极极化电位的升高,缓蚀体系的腐蚀电流密度有所增加, 最终进入与空白溶液极化行为相似的过程。但在相同阳极极化电位下,添加缓蚀剂时的腐蚀电流密度却明显小于空白体系,这种现象在山梨醇与SDBS摩尔比为1:3时更为明显。这是因为随阳极极化的增强,吸附在钢筋表面的缓蚀剂容易发生脱附,从而导致腐蚀电流密度有所增大。但由于缓蚀剂分子与钢筋表面铁离子所形成络合物的稳定存在,当吸附在钢筋表面的缓蚀剂分子发生脱附后,体系的腐蚀电流密度仍明显低于空白体系。而对于抗坏血酸与SDBS复配体系,上述缓蚀剂脱附现象并不明显,这可能是因为抗坏血酸在碱性溶液中可以解离出抗坏血酸根离子,与钢筋表面Fe2+、Fe3+离子的螯合作用较强,致使钢筋表面保护膜比较稳定[6]。由表2拟合结果可以发现,3种有机化合物在单独使用时对钢筋的缓蚀效果按山梨醇<葡萄糖<抗坏血酸的顺序递增;而分别与SDBS复配后,可以看出在研究浓度范围内,当山梨醇和葡萄糖分别以1:3摩尔比与SDBS复配,抗坏血酸与SDBS配比为1:1时,复配物对钢筋具有最好的缓蚀效果,其中,以抗坏血酸与SDBS配比为1:1时缓蚀效果最优。这与线性极化结果相一致。
表2 3.5% NaCl饱和Ca(OH)2 溶液中由动电位极化数据得到的钢筋电极电化学参数
| System | Ratio | Ecorr(mV) | I ( μA cm–2) | -βc (mV dec–1) | βa (mV dec–1) |
| Blank | -515 | 4.9 | 111 | 185 | |
| S | -605 | 1.6 | 109 | 201 | |
| SDBS | -619 | 0.6 | 103 | 206 | |
| S+ SDBS | 1:3 | -639 | 0.3 | 101 | 225 |
| S+ SDBS | 1:1 | -637 | 0.5 | 105 | 207 |
| S+ SDBS | 3:1 | -647 | 0.7 | 101 | 207 |
| G | -624 | 0.6 | 103 | 207 | |
| G+ SDBS | 1:3 | -653 | 0.5 | 101 | 205 |
| G+ SDBS | 1:1 | -667 | 0.7 | 104 | 202 |
| G+ SDBS | 3:1 | -652 | 1.1 | 102 | 206 |
| A | -692 | 0.3 | 118 | 205 | |
| A+ SDBS | 1:3 | -657 | 0.4 | 105 | 203 |
| A+ SDBS | 1:1 | -632 | 0.2 | 105 | 205 |
| A+ SDBS | 3:1 | -697 | 0.5 | 100 | 206 |
3.3 电化学阻抗
图 2 为 3.5% NaCl 饱和 Ca(OH)2 溶液中空白和添加不同缓蚀剂时钢筋电极的电化学阻抗行为,其中图2(a) 为山梨醇与SDBS复配时的阻抗结果,图2(b)为抗坏血酸与SDBS复配时的阻抗行为,葡萄糖与SDBS复配后的阻抗因与其类似,具体阻抗结果没有给出。可以看出,不论是在空白还是添加缓蚀剂的溶液中,钢筋的阻抗行为均具有2个时间常数的特征,分别对应着Nyquist 复平面上2个容抗弧。高频端容抗弧可归属与电极表面双电层电容对高频激励信号的响应, 反映钢筋电极表面/溶液界面的状态, 低频端的容抗弧则表征电极表面膜对扰动信号的响应, 其阻抗行为与膜的均匀性和致密性相关[4],这层膜主要由吸附的缓蚀剂分子、缓蚀剂与铁离子的络合物和腐蚀产物所构成,为一种复合性保护膜。故可用图3等效电路对钢筋的阻抗行为进行拟合, 其中, Rs为溶液电阻,Rct为电荷传递电阻,Rf代表电极表面形成的保护性复合膜电阻,由于钢筋电极表面的粗糙, 所测容抗弧常偏移理论行为, 故用常相位角元件 CPE 代替电容 C ,CPE1代表电极表面/溶液界面双电层电容, CPE2 代表电极表面所形成的复合膜电容, n 为表征电极表面不均匀程度的弥散系数, 拟合结果见表3。
由表 3 可以看出,添加缓蚀剂后,分别表征电极表面双电层电容和膜电容的Y0值减小,钢筋表面界面电容的减小说明缓蚀剂取代水分子吸附于金属表面。而添加缓蚀剂后Rf值的增大,说明缓蚀剂在钢筋表面的覆盖度增大,表面膜防护性能提高,钢筋的抗腐蚀能力增强。这一方面得益于化合物参与膜的形成,使其比空白溶液中形成的表面膜更加稳定、致密,钢筋耐 Cl−侵蚀性能提高;另一方面缓蚀剂分子也可直接吸附于裸露的钢筋表面,有效减少钢筋表面潜在的 Cl− 吸附活性点数量, 降低局部腐蚀发生可能。另外从表3还可发现,在单独使用时3种含氧有机物对钢筋的缓蚀效果按下列顺序递增:山梨醇<葡萄糖<抗坏血酸;而对于复配后的缓蚀剂,在实验配比范围内,可以看出,当山梨醇、葡萄糖分别与SDBS配比为 1:3,抗坏血酸与SDBS配比为1:1时缓蚀剂对钢筋电极具有最好的缓蚀效果,这与其它电化学实验结果相吻合。
#p#分页标题#e#
值得注意的是对单独添加和含有十二烷基苯磺酸钠的体系,与空白时相比,双电层界面电容明显减小,可能是因
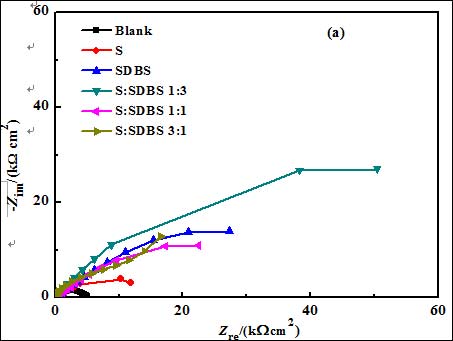
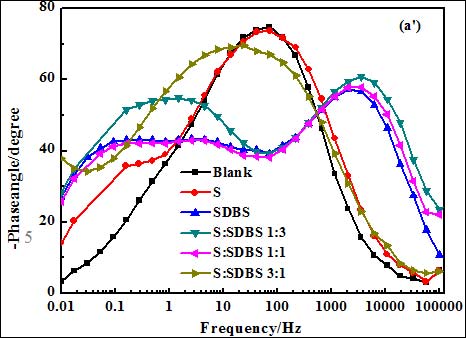
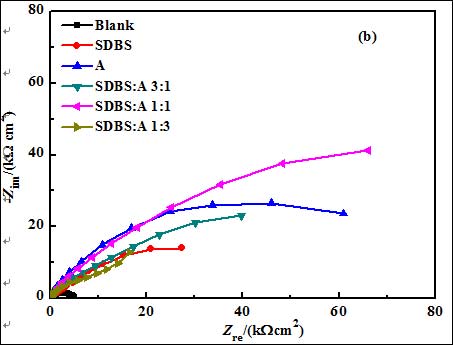
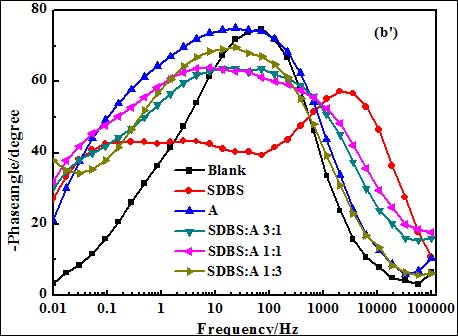
图 2. 空白和添加不同缓蚀剂时3.5% NaCl 饱和Ca(OH)2 溶液中钢筋电极的电化学阻抗行为
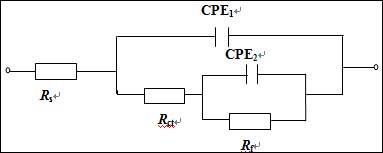
图3. 模拟等效电路图
由于十二烷基苯磺酸钠作为优良的表面活性剂可牢固的吸附在钢筋表面,有效地降低了电极界面的介电常数。另外,因SDBS具有较长的疏水烷基链,且在高浓度下自身可聚集而形成胶团,使其在钢筋表面吸附所形成的疏水层厚度要比单分子层吸附时要大,致使钢筋/溶液界面电容降低,类似结果也见文献报道[10]。这种现象可能与碱性条件下SDBS胶束的形成过程有关。众所周知,当表面活性剂在水溶液中超过一定浓度(临界胶团浓度)时,可自发聚集而形成具有烷基链缠绕的内核,外围被亲水头基环绕的胶团或胶束,从而改变了表面活性剂在金属表面的吸附行为,其具体机制还有待进一步探讨。
表3 钢筋在3.5% NaCl饱和Ca(OH)2 溶液中EIS 参数
| System | Ratio | Rs (Ω cm2) | CPE1-Y0 (μΩ–1.sn.cm –2) | n1 | Rct (Ω cm2) | CPE2-Y0 (μΩ–1.sn.cm –2) | n2 | Rf (kΩ cm2) |
| Blank | 10.8 | 33.2 | 0.93 | 1575 | 196.9 | 0.65 | 3.61 | |
| S | 9.2 | 29.1 | 0.91 | 1992 | 185.8 | 0.65 | 13.46 | |
| SDBS | 15.3 | 2.8 | 0.88 | 281 | 105.8 | 0.53 | 81.1 | |
| S+ SDBS | 1:3 | 8.5 | 4.9 | 0.82 | 423 | 59.6 | 0.66 | 96.3 |
| S+ SDBS | 1:1 | 13.7 | 5.0 | 0.83 | 347 | 77.3 | 0.57 | 57.8 |
| S+ SDBS | 3:1 | 10.8 | 5.0 | 0.83 | 323 | 120.3 | 0.53 | 56.7 |
| G | 12.8 | 28.5 | 0.89 | 2687 | 74.4 | 0.58 | 63.4 | |
| G+ SDBS | 1:3 | 9.12 | 4.0 | 0.85 | 371 | 95.2 | 0.55 | 97.7 |
| G+ SDBS | 1:1 | 10 | 4.6 | 0.86 | 344 | 100.8 | 0.56 | 61.3 |
| G+ SDBS | 3:1 | 13.6 | 4.7 | 0.85 | 283 | 138.7 | 0.48 | 35.1 |
| A | 4.7 | 26.4 | 0.8 | 6636 | 24.6 | 0.72 | 95.6 | |
| A+ SDBS | 1:3 | 11.8 | 5.6 | 0.91 | 684 | 59.8 | 0.61 | 70.3 |
| A+ SDBS | 1:1 | 10.0 | 5.4 | 0.93 | 576 | 40.6 | 0.67 | 117.7 |
| A+ SDBS | 3:1 | 9.4 | 10.1 | 0.88 | 498 | 98.1 | 0.66 | 49.7 |
3.4 量子化学计算
为更好地分析、了解缓蚀剂的作用机理,利用 Hyperchem 7.5 软件对3种含氧化合物和十二烷基苯磺酸根离子进行了量化计算,得到的相关分子结构参数列于表 4。其中缓蚀剂分子的硬度 (η) 与绝对电负性 (χ) 分别按下列公式计算[6,11,12]:

其中,I与A分别表征缓蚀剂的解离性能和电子亲和性能,EHOMO和ELUMO别为缓蚀剂最高占据轨道和最低非占据轨道能量。绝对电负性χ表征原子在分子中吸引电子的能力,是原子或离子形成价键能力的量度。绝对电负性越大,有机分子作为路易斯碱越硬;反之,则碱性越软[6]。根据这一原理,由表 4 可以看出,所研究的缓蚀剂作为路易斯碱的硬度按下列顺序递增:山梨醇~葡萄糖<抗坏血酸<十二烷基苯磺酸根阴离子。由此可对含氧化合物与SDBS的缓蚀行为做出很好的解释:存在氯离子的碱性 Fe-H2O体系中,金属表面存在不同的路易斯酸碱[7]:裸露的铁属于软酸,而腐蚀产生的铁离子或覆盖在钢筋表面铁的氧化物则属于硬酸。十二烷基苯磺酸根阴离子属于硬碱,容易与 Fe3+或 Fe2+ 配位形成络合物而覆盖在金属表面,从而抑制钢筋的腐蚀。抗坏血酸作为路易斯碱硬度与十二烷基苯磺酸根差别不大,也可与Fe3+或 Fe2+ 配位形成稳定的络合物,同时它还可通过分子中的羟基基团和五元环结构吸附在裸露的铁表面, 阻滞铁的阳极溶解。而山梨醇和葡萄糖作为路易斯碱硬度较小,与Fe3+或 Fe2+ 配位能力相对较弱,但它们却容易通过分子中的羟基或醛基吸附于裸露的钢筋表面而形成吸附膜,直接作为阻挡层来阻碍腐蚀性成分对钢筋的侵蚀。因此,山梨醇与SDBS间具有较好的缓蚀互补作用,从而使二者的复配物具有良好的缓蚀效果,提高了钢筋抗氯离子的侵蚀能力。葡萄糖作为路易斯碱的硬度与山梨醇相当,与SDBS复配后的缓蚀效率也有所提高,但提高程度却不如山梨醇。抗坏血酸作为3种含氧化合物中路易斯碱硬度最大的化合物,与SDBS复配后具有最好的缓蚀效果和良好的协同效应, 这与电化学研究结果相一致。
#p#分页标题#e#
表 4 缓蚀剂分子结构参数
| Inhibitor | EHOMO/eV | ELUMO/eV | η/eV | χ/eV |
| SDBS | -5.85 | 3.431 | 4.64 | 5.85 |
| S | -10.57 | 1.99 | 6.28 | 4.29 |
| G | -10.18 | 1.18 | 5.68 | 4.50 |
| A | -9.70 | -0.54 | 4.58 | 5.12 |
4 结 论
(1) 3.5% NaCl 饱和 Ca(OH)2 溶液中,3种含氧化合物单独使用时对钢筋的缓蚀效果遵循下列顺序依次增加:山梨醇<葡萄糖<抗坏血酸;在所研究的浓度配比范围内,当山梨醇、葡萄糖与SDBS摩尔配比为 1:3,抗坏血酸与SDBS配比为1:1时复配物具有最好的缓蚀性能,其中抗坏血酸与SDBS复配后缓蚀效果最好。
(2) 3种化合物与SDBS间均具有良好的缓蚀协同效应,其中抗坏血酸与SDBS间协同效应最好,这种协同作用与它们作为路易斯碱的硬度密切有关,据此可较好的解释化合物的缓蚀作用机制。
致 谢
本工作得到国家自然科学基金(51071161)及国家科技支撑计划(2007BAB27B03)的资助,特此致谢!
References
[1]K Saravanan, S Sathiyanarayanan, S Muralidharan, S S Azim, G Venkatachari. Performance Evaluation of Polyaniline Pigmented Epoxy Coating for Corrosion Protection of Steel in Concrete Environment[J]. Progress in Organic Coatings, 2007. 59(2): 160-167.
[2] Naifeng Hong,Development and Use of Steel Bar Inhibitor[J]. Industrial Construction, 2005, 135 (16): 68-70 (Ch)。
洪乃丰, 钢筋阻锈剂的发展与应用[J]. 工业建筑2005, 135 (16): 68-70
[3] H E Jamil, M F Montemor, R Boulif, A Shriri, M G S Ferreira. An Electrochemical and Analytical Approach to the Inhibition Mechanism of an Amino-alcohol-based Corrosion Inhibitor for Reinforced Concrete[J]. Electrochimica Acta, 48 (2003) 3509-3518
[4] Xin Zhou, Huaiyu Yang, Fuhui Wang, [BMIM]BF4 Ionic Liquids as Effective Inhibitor for Carbon Steel in Alkaline Chloride Solution[J]. Electrochimica Acta, 56 (2011) 4268-4275
[5] F Wombacher, U Maeder, B Marazzani, Aminoalcohol Based Mixed Corrosion inhibitors[J], Cement & Concrete Composites, 26 (2004) 209-216
[6] S Martinez, L Valek, I Stipanovi? Oslakovi?. Adsorption of Organic Anions on Low-Carbon Steel in Saturated Ca?OH…2 and the HSAB Principle[J], Journal of The Electrochemical Society, 2007,154(11) C671-C677
[7] M Yamaguchi, H Nishihara, K Aramaki. The Inhibition of Passive Film breakdown on Iron in a Borate Buffer Solution Containing Chloride Ions by Organic Anion Inhibitors[J]. Corrosion Science, 1994. 36(2): 241-258.
[8] E Machnikova, K H Whitmire, N Hackerman. Corrosion inhibition of carbon steel in hydrochloric acid by furan derivatives[J]. Electrochimica Acta, 2008. 53(20): 6024-6032.
[9] Fuguo Liu, Min Du, Effect of New Type Compound Inhibitor on Inhibition Behavior of Steel G105[J]. Acta Metallurgica Sinica, 2007. 43(9): 989-993(Ch)。
刘福国,杜敏,新型复配缓蚀剂对G105 钢在NaCl溶液中缓蚀行为的影响[J]. 金属学报2007. 43(9): 989-993
[10] Yujun Si, Zhongping Xiong, Changguo Chen, Minjiao Li, Xuesong Feng, Inhibiting Ability of Sodium Dodecyl Benzene Sulfonate to AZ31 Magnesium Alloy[J]. Rare Metal Materials and Engineering, 2007. 36(12): 2244-2247
司玉军,熊中平,陈昌国,李敏娇,封雪松,十二烷基苯磺酸钠对AZ31 镁合金缓蚀作用研究[J]. 稀有金属材料与工程2007. 36(12): 2244-2247
[11]R G Pearson, The HSAB principle - More quantitative aspects[J]. Inorganica Chimica Acta, 1995. 240(1-2):93-98.
[12]Ju Hong, Zhengpeng. Kai, and Yan Li, Aminic nitrogen-bearing polydentate Schiff base compounds as corrosion inhibitors for iron in acidic media: A quantum chemical calculation[J]. Corrosion Science, 2008. 50(3): 865-871.





















