科普|有关于化学腐蚀的相关知识
2018-03-20 11:16:40
作者:本网整理 来源:网络
题目1-----什么是电化学的腐蚀和速度控制过程?
题目2-----什么是电化学腐蚀?
题目3-----化学腐蚀与电化学腐蚀有何区别?
题目4----什么是化学腐蚀?
题目5-----一般来说有哪些防止金属腐蚀的方法?
什么是电化学腐蚀和速度控制过程?
腐蚀电池工作时,阳极过程、阴极过程、电子导电过程和离子导电过程这4个基本过程彼此串联,共同构成一个完整的电流回路。因此,腐蚀速度(即腐蚀电流密度)取决于腐蚀电池中阻力最大 、最缓慢的基本过程,这一过程就是电化学腐蚀的速度控制过程。如果能增大速度控制过程阻力,就可有效地减小金属的腐蚀速度。例如,停炉保护时经常采用的热炉放水、余热烘干方法就是通过增加离子导电过程的阻力来控制锅炉金属的腐蚀。
什么是电化学腐蚀?
电化学腐蚀是指金属表面与电解质发生电化学作用而引起的破坏。在电化学腐蚀过程中,金属的氧化(阳极反应)和氧化剂的还原(阴极反应)在被腐蚀金属表面的不同区域上同时进行,电子可通过金属基体从阳极区流向阴极区,从而产生电流。例如,碳钢在酸中腐蚀时,在阳极区铁被氧化为Fe2+ ,所释放的电子通过钢的基体由阳极(Fe)流至阴极(Fe3C)表面,被H+吸收而产生氢气,即发生下列腐蚀反应:
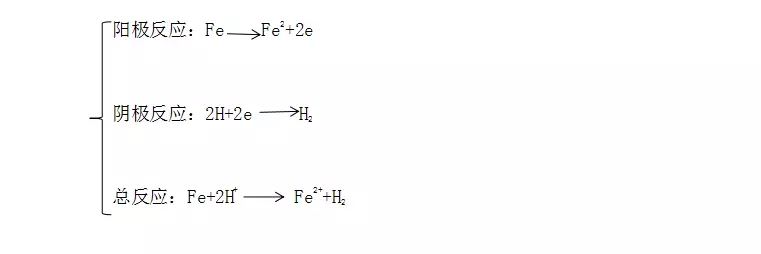
可见,电化学腐蚀实际上是一种短路原电池反应结果,这种短路原电池称为腐蚀电池。也由于阴极与阳极短路(往往是通过被金属的基体),腐蚀电池反应所释放的化学能不能对外界作任何有用功。
电化学腐蚀的实例很多,各种湿腐蚀及熔盐腐蚀皆属此类,热力设备的腐蚀绝大部分分属于电化学腐蚀。
化学腐蚀与电化学腐蚀有何区别?
从化学反应类型来看,无论化学腐蚀,还是电化学腐蚀都属于氧化一还原反应,这是两类腐蚀的共同之处。但是,两者间的区别主要是金属和氧化剂之间的作用机理不同,具体可归纳列于表:
化学腐蚀和电化学腐蚀的比较
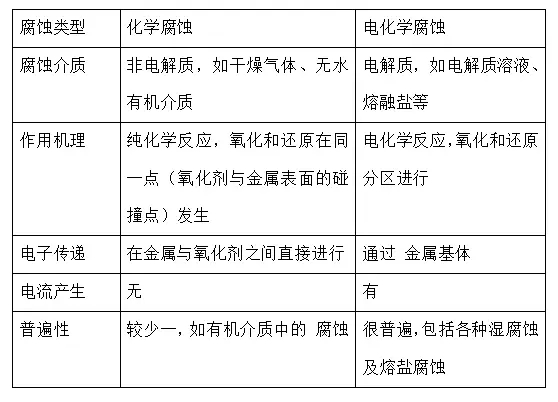
什么是化学腐蚀?
化学腐蚀是指金属表面与非电解质直接发生纯化学作用而引起的破坏。在化学腐蚀过程中,非电解质中的氧化剂在一定条件下直接与金属表面原子发生氧化还原反应而生成腐蚀产物,反应中电子的传递是在金属与氧化剂之间直接进行的,所以没有电流产生。单纯化学腐蚀的实例较少,金属在有机介质中的腐蚀属于化学腐蚀,但这种腐蚀往往因介质含有少量水分而转变为电化学腐蚀。
一般来说有哪些防止金属腐蚀的方法?
通常,防止金属腐蚀应从提高材料的耐蚀性、消除产生腐蚀的条件和减小介质的侵蚀性等方面来考虑,主要有合理选材和腐蚀设计、表面保护设计、介质处理和电化学保护技术。
1.合理选材与腐蚀设计。合理选材主要是根据材料所要接触的介质的性质和条件,材料的耐蚀性能和价格,选择在这种介质中比较耐蚀、满足设计和经济性要求的材料。
防腐蚀设计主要是防蚀结构设计和防蚀强度设计。防蚀结构设计的原则包括:结构件的形状应尽可能简单,消除发生各种局部腐蚀的条件等;防蚀强度设计主要是对全面腐蚀的腐蚀裕量的选择,以保证金属结构的寿命要求。
1. 表面保护技术。表面保护技术就是利用各种表面覆盖层(金属镀层或非金属涂层)将金属与腐蚀介质隔离而使金属得到保护。
2. 介质处理。介质处理的目的是降低介质的腐蚀性,促使金属表面钝化。通常可采用下列方法①控制介质中溶解氧等氧化剂的浓度;②提高介质的ph值;③降低气体介质中的湿分;④向介质中添加缓蚀剂。
3. 电化学保护。电化学的保护可分为阴极保护和阳极保护两种方法:①阴极保护。阴极保护是将金属作为阴极,利用阴极电流使金属电极电位负移、阳极溶解速度减小从而得到保护。它又可分为牺牲阳极保护和外加电流阴极保护。在火力发电厂,凝汽器水侧管板和管端部等的防护均可采用阴极保护。②阳极保护。阳极保护是将金属作为阳极,利用阳极电流使金属电极电位正移,达到并保持在钝化区内从而得到保护。阳极保护只适用于可能发生钝化的金属,如碳钢浓酸贮槽的阳极保护。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。